短期間で結果が出ない受験勉強の不安をなくす方法
こんにちは。
はるです!
やっぱりいくら勉強を続けても、
なかなか模試で点数が上がらない
と不安になることありますよね。
僕もそんな1人でした。
今の勉強は
3ヶ月後に成果がでるから
安心しろ!
学校でも塾でも先生はそんなふうに
励ましてくれますよね。
でも、
今の勉強が正しいのか
間違っているのかわからない。
結果が出なかったらどうしようと
やっぱり不安で仕方ない。
僕も悩みました。
なので今回は、
「あるたった1つの方法」
をやり続けるだけで、
あなたが
結果の出ない受験勉強で
不安を感じなくする。
そんな方法を伝授します!

なんで、
あなたが
模試の点数が上がらないことに
不安になったり、
結果のだせる勉強になっているか
と考えてしまうのはなぜでしょうか?
それはあなたが目先の模試の点数に
左右され、
勉強時間と学習してきた努力を
見ていないからです!
つまり、
「自分の努力」
が目に見えていないから、
そしてこの「自分の努力」を
日々の受験勉強で、
見える化することが、
受験勉強をやり続ける
たった一つの方法です。
これをやることで、
友達や他人の意見に
どうこう言われても
動じずに
模試の点数を受け入れ、
模試の点数に
浮かれたり、沈んだりすること
がなくなります。
イメージをつかんでもらうために
僕の例をお話しすると、
僕は元々、
化学の定期テストでは
平均より上回り
友達よりもできていました。
しかし、模試になると
友達よりも低い点しか取れませんでした。
そのせいで、
模試のできる友達には
E判定!
とバカにされていました。
すごい悔しかったです。
そんな時、
有名私立大や有名国立大に
何人も輩出している
塾講師の先生が
やる気の継続法を
教えてくれました。
その先生の授業は面白く、
授業の合間にする雑談では
やる気を出させてくれる言葉を
送ってくれました。
成果も出していて、
やる気が継続する授業を教えてくれる
先生がいうことなら間違いない
と思い、
僕はその人が言うことの
・1円貯金
と
僕なりに考えた
・ボールペン活用術
・スマホをいじらなくするアプリを使う
を継続しました。
特に、ボールペン活用術は
受験勉強をするときは
ボールペンで問題を解き、
使い切った芯を貯めて
どれだけ書いたのかを
見える化しました。
1円貯金とは
2時間勉強したら1円を
500mlのペットボトルに貯金していき、
貯金したお金は
受験が終わったらユネスコに寄付する。
というものです。
何時間勉強したのかを
1円貯金とアプリで見える化しました。
こうすることで、不安を減らし
受験本番前に
貯まった1円とボールペンの芯を見て
僕は
これだけやったんだ!
努力は裏切らない!
と自信を持って
受験に望むことができました。
この効果は本当に
馬鹿にできないです。
もしあなたが
「今の勉強で結果が出るのか不安」
そう思うのならば、
絶対に取り入れて勉強しましょう。
今からやってください。
まずは、
シャーペンからボールペンに
持ち替えて問題を書いてみましょう。
間違えても、バツでいいんです。
間違えても、
それが努力ですから
口で文句ばかり言ってる人は気にしない。
目に見える自分の努力を
積み重ねてください。
志望校合格目指して
頑張っていきましょうね!
はるでした!

化学はパズルのピース
こんにちは。
はるです。
化学はどこから勉強したらいいか
わからない
と悩んだことありませんか?
理論が化学の基礎だから
完璧にするぞ!
と意気込んで勉強したものの
模試の点数が思ったより上がらない
そんな経験ありませんか?
実は化学の勉強に
知らないと
やりがちな思い込み
があるからなんです

この考えを知っていれば
化学の勉強が楽しくなり
重くてやり出せない
勉強のスタートが軽くなり
化学が得意科目になります!
この考えを知らなかったが為に
なかなか点数の上がらない化学に
自分は頭が悪いんだ、、、
化学は苦手なんだ、、、
こんな勉強つまらない!
と自分にも化学にも嫌気がさしたまま
苦しみだけが蓄積されます。
あなたにはなんの非もないのに、、、
あなた自身も、
化学にも好きになってほしい

化学の勉強に希望と
あなたの伸びしろを感じさせてくれる
考えは、、、
化学は
パズルのピース!

勉強を続けていれば
ある時突然点数が爆上がりする科目
だからです!
僕も悩みました。
化学はもともと好きでした。
しかし、受験勉強すればするほど、
模試で点数が変化しないことに
ショックで、
嫌いになりそうでした。
でも、絶対合格したい!
そんな気持ちで勉強を続けた結果、
最初の3ヶ月は30点、30点、30点が
45点、60点と上がっていき、
センター本番は80点!
模試で30点しか取れなかった
僕も50点upできたんです。
化学はパズルのピース
とはどういうことか?
端的に言うと
理論・無機・有機化学
バランスよく勉強しないと
点数は上がらないです。
化学の勉強の
イメージはパズルのピース!
パズルしたことありますか?
完成図を見ないでやりだすと
何を作っているのかわからないですよね?

でも、かどや端のピース
を埋めて、色と形で何となく
少しずつ埋めていくと
何の絵なのかわかってきます。
そして、
パズルの全体像がわかって
猫のパズルか?犬のパズルか?
とわかると、
あとはあっという間に
完成できますよね。
化学も同じです。
理論~無機~有機~
酸化還元~硫酸の性質~糖の分解~
それぞれが一見
関係がないように見えますが
実はすべてが関係しています
だから、パズルだと思ってください!
わかるところから
ピースを埋めて
知識を増やしていけばいいんです!
そして、
全体の関係性が見えてきたとき
模試で点数が上がりだすのです。

化学が楽しくなって、
模試の点数が60、70、80点と
上がっていい流れができたころには
受験で通用する
レベルになっています。
不安は少しなくなりましたか?
化学を得意科目にしちゃいましょう!
やるべきことは分かりましたよね?
今すぐ、スマホを机の隅っこにおいて
ペンをもって、問題集をやってみましょう!
3つの濃度の違いわかりますか
こんにちは。
はるです。
濃度の計算はいくら勉強しても
テスト本番になると
捨て問題になるんだよなー
そういう経験ありませんか?
モル濃度に質量モル濃度に
質量パーセント濃度、、、
公式3つも覚えられないよ!
と悩んだことありませんか?
質量パーセント濃度
モル濃度
質量モル濃度
の違いを理解して覚える方法があります!

この方法を知っていると
濃度の計算が楽勝になり
3つの違いも分かって
応用問題も簡単に解けるようになります。
もしこの方法を知らないままでいると
はい、濃度の計算は捨て!
また、公式忘れたから解けない!
解けても時間がかかる
こんな嫌なことの繰り返し
続けたくありませんよね?
実は
3つの濃度計算は
その言葉の意味と用途
単位をみれば一目瞭然なんです!

まずは、それぞれの違いを知ることで
理解を深めることができます。
では、違いを見ていきましょう。
① 質量パーセント濃度(%)
その名の通り、質量の割合です。
溶液100g(内容量全部の重さ)中の
溶質の質量(g)です。
例で考えてみましょう。
1学年100人のうち
Aクラスの人数が25人だとしましょう。
Aクラスは25%ですよね?
塩15g入れて、塩水100g作ります。
全量は水と塩
すなわち塩水100g
知りたいのは塩の割合
塩15g
なので質量パーセント濃度は15%
全量(100g)に対しての
知りたい溶質の重さの割合ですよね
溶質(g) ÷ 全量(100g) × 100 (%)
だから、質量パーセント濃度なんです

また、求めたいのは塩!溶質!
主語に着目してください。
質量パーセント濃度は
温度変化を伴うときによく使います。
再結晶なんかの問題ですね。
② モル濃度(mol/L)
単位を見てください!
「/L」は毎リットル、
「1L中に」ということです。
23mol/Lなら1L中に23mol
注意は
溶液(溶媒+溶質)が1L
なぜ溶液なのかというと
もし溶媒、例えば水にしたとき
1L測るの簡単ですよね?
あまり意味がないからです。
モル濃度は一度溶液を作ったら
化学の計算では必須の
モルがわかるため、
とても便利。

③ 質量モル濃度(mol/kg)
溶媒1kgに何molあるのか?
を表しています。
正確には溶媒と溶質のモル比です。
これは
混合物、砂糖水などの性質を知るうえで
基準が水1kgだと正確に比べられます。
そのため、混合物の凝固点降下
などでよく使います。
問題は計算方法ですよね
ズバリ、単位計算です!
モル濃度を例にやり方を説明します。

上のように
モル濃度の単位(mol/L)から
計算式はわかるんです。
あとは、方程式として解くだけ!
だから計算は簡単です!
濃度の計算方法をステップ化してみます。
①問題では何を求めたいのかをチェック
②単位を使って計算式を作る。
③あとは計算するだけ!
ここで、難しい問題になると
単位換算をしないと
解けなくなります。
ですが!
応用を効かせた単位計算を使うと
簡単に単位換算の仕方がわかります!
次回は単位換算についての
秘密をお伝えします。

とはいえ、基本の
濃度の計算って問題によく出てきますよね
まずは問題集を開いて
簡単な質量パーセント濃度の問題
1問を解いてみましょう!
さぁ、ペンをもって解いてみよう!
モル計算はむしろラッキー問題
こんにちは。
はるです。
テストで物質量モルの
計算は時間かかるからと
後回しにした経験ありませんか?
久しぶりに、模試で問題が出て
計算の仕方忘れて
解けないことありますよね。
実はあることを知っていると
物質量モルの
3つの公式を暗記せずとも
計算式が立てられて
簡単に解けるようになる
そんな方法があるんです!
この方法を使うと
モルの計算がラッキー問題に感じ
計算系全般が解きやすくなり
安定した得点源ができる
ようになります。

この方法を使わないと
モルの計算問題は捨てる
計算系の問題はあきらめ
用語問題でしか点が取れない
そんな悲しい未来が待ってます。
そんな未来嫌ですよね?
ある方法とは
ズバリ、
単位計算をすることです!
実は化学のほとんどの計算問題は
問題文に載っている
答えの単位(mol、g、L)
と計算に使う単位(g/mol、L/mol)
から計算式がわかってしまうのです!
そして、物質量モルなら
質量・粒子数・体積と物質量の
関係図を理解し覚えることで
計算がめちゃくちゃ楽になります!
これが関係図です。

※字が汚いですが、、、
この図は書いて
覚えてください!
この図のポイントは
1 質量、体積、粒子数が
すべて
物質量モルとつながっている
→とりあえずmolになおす!
2 つながり方が
質量はモル質量(g/mol)
体積は標準状態の気体
1molあたりの体積(22.4L/mol)
粒子数は
アボガドロ定数(6.0×10^23/mol)
3 単位の見方
モル質量なら下の図のように
見れるようにしてください。

注意点は
1 モル質量は
分子量、原子量、式量によって変わる。
ようするに、O₂、H₂Oなど
物質によってかわる。
2 体積は気体で標準状態!
(0℃、1013hPa)
ようするに、
水など液体だと適用されない!
3 粒子の数の個
化学では個という単位がないので
アボガドロ定数の単位(/mol)
いうなれば、(個/mol)です。
ん~これじゃあよくわからない、、、
と思うかもしれません
・・・が!
以下のステップでやってみてください。
①問題文の単位だけをみる
例、酸素分子1.2×10^23個の
体積は標準状態で何Lか?
原子量:O=16
アボガドロ定数:6.0×10^23/mol
②単位計算
まずは、単位の過程
一度モルに変換!
例、 個 → mol → L
次に単位だけで計算式を導く。

問題文にアボガドロ定数、22.4L/mol
は書いてないこともあるので
関係図はしっかり覚える。
関係図より、
個 → mol
6.0×10^23/mol

上の単位計算より
個 ÷ 個/mol = mol
mol → L

上の図のように
mol × L/mol = L
合わせると、
個 ÷ 個/mol × L/mol = L
③あとは数値で計算するだけ!
例
1.2×10^23 ÷ 6.0×10^23 × 22.4
関係図とこの3ステップ
だけでいいんです!
どうですか?できそうですよね?
今すぐできます!
まずはかばんから
化学の問題集をだして
(1)番 だけでいいです、
単位だけ見てください!
周期表のちょっとエッチな覚え方
こんにちは。
はるです。
周期表って問題によく出てくるけど
全部は覚えてないから解けない
そんな経験ありませんか?
すいへいりーべいー・・・これじゃ全部覚えられない
他のおぼえかたないの?
といろいろネットで調べたことありますよね?
ちょっとエッチで、、、
もっとインパクトがあって
すいへいりーべいー・・・だけよりも
覚えやすい
そんな周期表の覚え方みつけました。
この覚え方を使うと
楽しく覚えられて
全く苦じゃなく
速く覚えられます。
すいへいりーべいー・・・
よりも多く覚えられる!
この覚え方を使わないと
毎回覚えなおしたり
すいへいりーべいー・・・
の先の元素が覚えられなかったり
いつになっても化学の基礎が覚えられないから
苦手のまま!
そんなのいやですよね。
周期表の覚え方とは
周期表の縦と横で
複数の語呂を使って
自分で表を完成させて
覚える!です。
複数の語呂で、
縦と横で覚えることで
語呂を一つ忘れても
周期表を完成させることができるからです。
さらに、ちょっとエッチな用語
なんだかんだ
みんな大好きだと思ってます。
最初にはっきり言っときますが
僕はいたって健全です!
大前提となる語呂と
縦と横の複合の仕方を教えます。

①横の覚え方
原子番号1~36番の語呂
|
H |
He |
|
水 |
兵 |
|
Li |
Be |
B |
C |
N |
O |
F |
Ne |
|
リー |
ベー |
ぼ |
く |
の |
お |
ふ |
ね |
|
Na |
Mg |
Al |
Si |
P |
S |
Cl |
Ar |
|
なな |
まが |
ある |
シッ |
プ |
ス |
クラ |
― |
|
K |
Ca |
Sc |
Ti |
V |
Cr |
Mn |
Fe |
Co |
|
ク |
閣下 |
スコッ |
チ |
ばあさん |
くろい |
ま〇こに |
手ェつ |
っこみ |
|
Ni |
Cu |
Zn |
Ga |
Ge |
As |
Se |
Br |
Kr |
|
2(に) |
度(ど) |
あえぐ |
が |
げろして |
明日 |
千(せん) |
秋(しゅう) |
楽(らく) |
ここだから、教えられますが、
塾などでは教えられない言葉ばかりです。。。
今までのすいへいりーべいー・・・
に付け足して覚えてください!
②縦の覚え方
上の周期表の族ごとに語呂があります。
<1族>
|
H |
Li |
Na |
K |
Rb |
Cs |
Fr |
|
エッチで |
リッチ |
な |
K君が |
ルビー |
せしめて |
フランスへ |
※最初の4つは覚えて!
<2族>
|
Be |
Mg |
Ca |
Sr |
Ba |
Ra |
|
ベットに |
もっぐて |
彼と |
すると |
バ |
ラいろ |
※最初の3つは覚えて!
<13族>
|
B |
Al |
Ga |
In |
Tl |
|
B |
ある |
が |
インポ |
立たず |
※ BはエッチのABCのB。
ちなみにAはキス、Bは愛撫、Cは挿入だそうです。
<14族>
|
C |
Si |
Ge |
Sn |
Pb |
|
短(たん) |
径(けい) |
ゲル(でる) |
寸止めで |
なま |
※短径はそちんです。
<15族>
|
N |
P |
As |
Sb |
Bi |
|
任(にん) |
婦(ぷ)の |
ア |
ソコは |
びろびろ |
<16族>
|
O |
S |
Se |
Te |
Po |
|
おくちに |
いっぱい |
せいしで |
てる |
ポロン |
※ほかにも語呂はあります。
<17族>
|
F |
Cl |
Br |
I |
At |
|
ふ |
くろ |
ぶらぶら |
私に |
当てて |
<18族>
|
He |
Ne |
Ar |
Kr |
Xe |
Rn |
|
変な |
ねえちゃん |
荒れ |
狂う |
奇声の |
乱発 |
※ハロゲン元素は最重要です!
友達には刺激が強すぎるので
他言無用でお願いします。
③ ①と②を使って、ゼロから周期表を作る。
まずは横に族番号1~18を紙に書き、
①をベースに表に書く。
②を使って書き加える。
最初は周期表を見ながら、
語呂と照らし合わせて書いてみる。
横で覚えきれなくても、
1~18の族番号と縦の語呂を使えば
かけるようになります!
気負わずに覚えた元素から
書いてみることが大事!
今から
ペンをもって
水平リーべー・・・と唱えながら
元素を紙に書いてみてください!
理解の深め方
こんにちは。
はるです。
暗記はできるけど、
理解の深め方は分からない
そう感じたことありませんか?
どうしても理解して覚えられない
そんなふうに悩んだことありませんか?
実はあることをすれば、
理解の深め方がわかるんです!
もし、用語の理解が深まったら?
受験や模試の
応用の効いた問題が解けるようになり、
定期テストレベルを脱することができます。

そのまま、理解しようとせず、
放置したら、
いくら勉強しても
模試の点数がなかなか上がらない
挙句の果てに勉強が嫌いになり、
やらなくなってしまいます。

理解を深めるとは、
長期的な記憶になり、
応用が利くようになります。
例えば、イオン化エネルギー。
模試や受験で
意味を直接聞かれる問題は
ほとんど出ません。
イオン化エネルギーという言葉が
問題文の一部となっています。
しかし理解していないと、
問題を解く段階にも入らないのです。

以下の問題は、実際の入試の一部です。
(問題)
第二周期の原子のうち、
イオン化エネルギーが最も大きいものはフッ素である。
〇か×か?
これは、正誤問題の一部です。
用語の意味をただ単に覚えているだけでは
全く解けませんよね?
これが、
塾講師になったつもりで友達に説明できるなら、
解けるはずです。
では、どうやって理解を深めればいいのか?
次のステップを踏んでみてください。
①その用語が、実際の問題(模試、問題集)で
どう出題されているのか、また資料集
を見てみる。
例、イオン化エネルギーは電子親和力と比べられる問題や
グラフ付きの問題でよく出ている。

②答えの解説を見てみる。
例、記事中間の(問題)解説、
答え、〇
③問題文中の対象用語以外の言葉から
どう理解すればいいかを考える。
グラフや図がポイントになる。
例、(問題)では第二周期の原子がポイント。
周期とは周期表のことを言っているので、
照らし合わせて考えてみる。
④用語の説明文と③のヒントを照らし合わせ、
教科書や資料集、参考書、ネットで
グラフや図表から理解。
例、イオン化エネルギーは原子から電子を一つとるのに必要な力。
が強い。
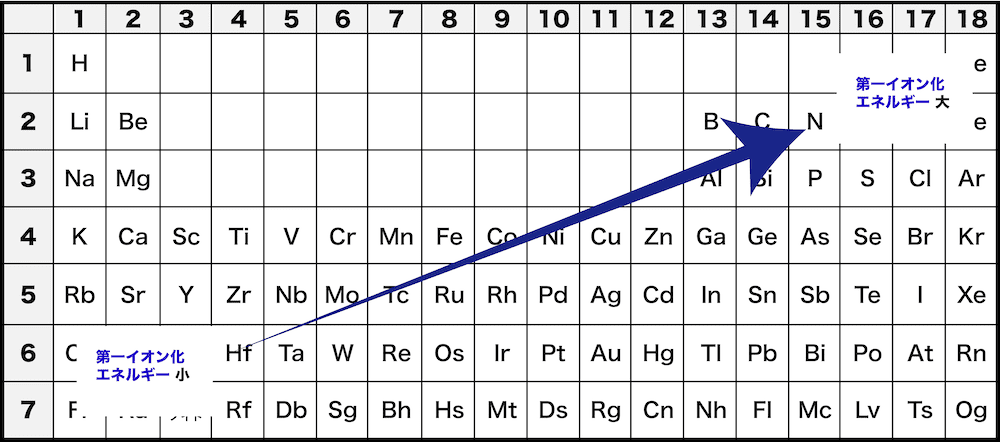
④は最初、自力でやるのが難しく
今までの知識とつなげていく必要がある。
これから、理解を深めにくい用語などについての
記事を書いていきます!
なので、まずは
①~③をやってみよう。
今から
問題集を開いて
理解を深めたい用語の
実際の問題をみてください!
理解と暗記を分ける
こんにちは。
はるです。
高1、2年のうちから受験勉強しても
どうせ忘れるし、やる意味ない!
そんな高校生はこの記事を読んでください!
今日は、新しく習う用語を
理解する部分と暗記する部分
に分ける方法を教えます。

理解と暗記を自分の中で分けられるようになると
暗記しなくてはいけない、、
そう思っていた部分が圧倒的に少なくなり、
効率が上がります。
そして、高校3年生から必死に勉強しなくても
いつも通りの勉強で
受験に合格できる

暗記力のある人はこう思ったことでしょう
定期テストの点数高いし、
受験も暗記してればできるし!
そうですね、暗記力には個人差があり
そんなあなたは優秀なのでしょう
しかし、
ずっとは覚えていられません
もし、理解と暗記に分けないで勉強してしまうと、
高3になって、問題集を解いていると、、
あれ、これなんだっけ?
こんな簡単な問題なのに解けない。。。
解説を見て、思い出した!
時間かかったけど、やっと理解できた!
でも、化学ばかりに時間さけないし
時間ないし、どうしよう、、、
高1、高2のときは勉強できたのに
どうして、、
っと、きっと後悔します

どうして理解する部分と暗記する部分に分けたほうがいいのか
暗記は学習において
必要不可欠であり、
暗記していないと、テストで点が取れないです。
そして、用語、水素などもう暗記するしかないものもあります。
理解は
一度わかってしまえば、
覚えやすくなり、なかなか忘れない。
また、理解して理屈がわかっているから
応用できるのです。
受験勉強に関しては、
理解して覚えることがベースとなります。
二つの良さを生かして
理解をベースとした勉強をし、
テストや模試の直前は
暗記分野を復習する。
そのために、
理解分野と暗記分野に分けて
勉強する必要があるのです。

実際に、どう分ければいいのか?
をステップ化して教えます。
①覚えたい用語、理論を決める。
学校で使っているノートでOK。
すでに書いた用語を一つ決める。
例、元素、イオン化エネルギーについてわけてみる。
②用語名と説明を色分けする。
緑(理解)、青(暗記)など二色のペンで色分け。
例、元素 物質を構成する基本構造。
イオン化エネルギー 原子から電子を取り除き、
一価の陽イオンになるのに必要なエネルギー。
③理解度チェック
塾講師になりきって、
友達に説明できるかどうかでわける。
例、元素は H、O、Cみたいな物質のもと → 理解OK
イオン化エネルギーは、、、→ 理解不足!
自分なりの言葉で説明できればOK!
できなかった用語などは
理解を深める必要があるが
ここでは分けて、
見える化することが大事。
別の記事で理解の深め方を教えます。
まずは、ノートを開いて
二色の色ペンを使って用語と説明分を色分けしてみよう!